Прочее про химические тепло и энергию (странности)
Везде ниже джоули и калории при реакциях рассчитаны, используя данные из Гурвич «Энергия разрыва химических связей. Потенциалы ионизации и сродство к электрону»:
https://drive.google.com/file/d/0B3i2SFYLER0Hb3Yyc1NQd0pJVG8/view?usp=sharing
Метод взят отсюда:
http://www.slideshare.net/ozlmgouru/ss-59522004
Известно, что активный металл Zn растворяется соляной кислотой HCl:
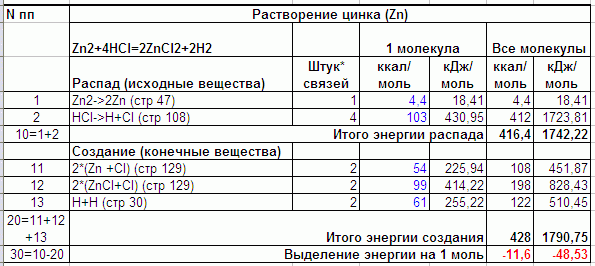
Получается, что реакция поглощает тепло. Может, конечно так оно и есть, а может сыграли свою роль плюс/минусы из таблицы (т.е данные не точные).
Медь в обычных условиях не растворяется соляной кислотой, хотя судя по расчету явных энергетических причин для НЕ образования CuCl или CuCl2 нет:
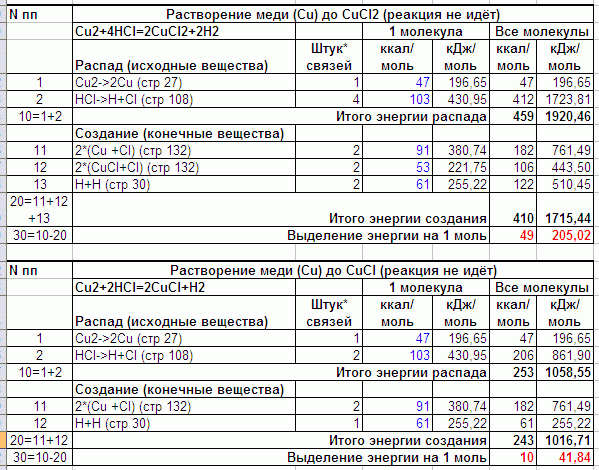
Энергия связи для меди (47) намного больше, чем для Zn (4.4) но её бы хватило на формирование новых молекул и в первом и во втором случае. Если бы сформировался CuCl2 ещё бы и в воздух много выделилось, но реакции не идут при обычных условиях.
А вот если добавить температуру (500-600):
http://chemiday.com/reaction/3-1-0-4837
Или кислород:
http://chemiday.com/reaction/3-1-0-4225
… в качестве своеобразного катализатора, то реакции, как и с перекисью:
http://akostina76.ucoz.ru/blog/2017-01-30-3805
… пойдут.
При этом 500-600 градусов не похожи на погрешность в 41.84 кДж из второй таблицы и как будет балансироваться энергия при реакции с добавлением тепла непонятно.
При воздействии кислорода реакция будет выглядеть так:

Из всего этого вывод: энергетический баланс, похоже не даёт ответа на то пойдёт реакция или нет, т.е, если смотреть на цифры, то нагрев вещества при недостатке энергии на образование новых веществ не гарантирует, что реакция пойдёт. Хотя по факту довольно часто происходит именно это. Довольно соблазнительно было бы определять по такой таблице, насколько надо нагреть, чтобы эти ионы переместились в нужные места, но, увы.
Возможно, что тепло, как и окислитель-кислород дают начальный импульс на разрыв металлической связи, которая у Cu на порядок больше чем у Zn.
Но и тут странность. Тогда уж ряду активности металлов логично совпадать с ростом силы связи для металлов. Но и это не так. Понятные и привычные металлы в порядке убывания активности:
Al (41, стр 19)– Zn (4.4, стр 47) – Fe (24, стр 28) – Cu (47, стр 27)– Ag (43, стр.19)– Au (38, стр.19).
Точно можно утверждать, что Zn и Fe очень сильно отличаются от примерно одинаковых остальных.
И уж совсем загадочно выглядит нейтрализация едкого натра (NaOH) соляной кислотой (HCl) потому что такой реакции точно надо идти с выделением энергии:

… а тут получается, что энергия итоговых веществ больше энергии исходных потому энергию надо поглощать извне для этой реакции а не выделять. (???).
Возможно я что-то всерьёз не понимаю. А возможно никакой поваренной соли в виде кристалла не формируется, а раствор энергию не поглощает. Кстати, так и не поняла, почему растворённые в воде соли, окрашивающие индикатор в фиолетовый цвет:
http://akostina76.ucoz.ru/blog/2017-01-30-3804
… и сигнализирующие о высоком pH безвредны для кожи. Возможно, эти вещи как-то связаны.
p/s
Это пример массы вопросов без ответов. А пока нет ответов весьма перспективный инструмент (т.е балансировку уравнений по энергиям) нельзя использовать ни для предсказания пойдёт реакция или нет ни для расчета выделенной и требуемой энергии.
|









